广东省人民医院 广东省肺癌研究所 张绪超 吴一龙
9月底的西班牙马德里时值秋季,阳光明媚,景色迷人。第39届欧洲肿瘤内科学会(ESMO)年会在此召开,约1.7万来自全球的专家学者参会。当今肿瘤学已经深入向分子分型和靶向治疗方向发展,本次大会也特别将主题定为“癌症的精准医学”。笔者有幸在中国临床肿瘤学会(CSCO)现任主任委员吴一龙教授的带领指导下与团队一同参会,现将本年度ESMO会议的肺癌部分进展总结如下。
异质性:肿瘤在时间和空间上进化的复杂性
本次会议在多个场次中均有肿瘤异质性的专题教育讲座或研究报告,对肿瘤分子变异在时空分布异质性的讨论较为全面而深入,有助于我们对肿瘤分子进化的理解,提示在做转化性研究、分子诊断、临床试验、耐药分子变异监测时均应考虑到异质性存在的普遍性和复杂性,而提高分子分析的敏感度(深度)及扩大基因谱分析对于准确获得异质性分布的信息很重要。
肿瘤存在时空分布异质性
伦敦大学学院的斯旺顿(Swanton)教授具体阐述了肺癌等实体瘤的同一病灶内部不同区域(即瘤灶内)分子异质性广泛存在。这种空间上的亚克隆分子异质性给临床诊断和靶向治疗药物的选择带来挑战。
肿瘤不仅在空间分布上存在较大的分子变异谱异质性,在肿瘤进化的过程中,时间上的动态分布变化也明确存在。瘤灶内不同区域亚克隆的平行进化往往会发生在同一基因的不同位点或同一信号通路的不同基因,针对这样的肿瘤分子异质性演变还是能够找到潜在的靶向治疗方法的。
肿瘤分子异质性发生的驱动因素在肿瘤演进的不同时点上可能不同,从而导致各时点特有的分子变异出现,进一步会促进时空的分子异质性出现。癌细胞的基因组倍增可能在肿瘤病程中或早或晚发生,进一步加剧基因组不稳定而导致细胞间异质性,这类肿瘤预后也相对较差。
空间上亚克隆区域驱动基因异质性的存在使得临床上单药疗效似乎有限,两项正在进行中的研究――TRACERx和DARWIN旨在分析肺癌时间上的分子进化和亚克隆驱动基因变异与疗效的关系,在未来会带来更细致的分析结果。
分子异质性的“树干-树枝”分布模型
Swanton研究组的贾梅尔(Jamel-Hanjani)汇报了非小细胞肺癌基因组变异进化结果,采用二代测序技术对3例肺鳞癌、8例肺腺癌、1例腺鳞癌、1例未分化肺癌的病灶多个区域进行分析,发现存在广泛的空间分子变异分布异质性,与富特雷尔(Futreal)刚发表在《科学》(Science)杂志上的11例肺腺癌同一病灶内不同亚克隆区域的分子变异分布非常相似,76%的分子突变在多个区域共存,其他分子突变存在空间分布异质性,预后差的患者往往具有较强空间分子异质性。
英国剑桥大学的卡尔达斯(Caldas)及癌症研究所的亚浦(Yap)分别总结了肿瘤的瘤内和瘤间(不同个体)分子异质性分布特点及对药物研发和临床研究的影响,指出有些肿瘤的分子变异可能是按不同空间区域分布,也有的肿瘤存在更复杂的异质性分布,即携带有不同驱动基因变异的肿瘤细胞并不是按照空间区域独立成群分布,而是不同分子变异的细胞交织在同一个区域,使得分析肿瘤的分子异质性及进化更加困难;同时也提出了将来以循环游离DNA或循环肿瘤细胞进行肿瘤疾病进程中的分子异质性或分子进化分析的可行性。

ERCC1等化疗相关标志物再遇“滑铁卢”
ERCC1预测含铂化疗疗效试验再次失败
结合本次会议公布的ET研究以及去年美国临床肿瘤学会(ASCO)年会公布的两项研究,我们可以得到如下启示,开展化疗分子标志物的检测及其指导化疗的临床研究尚不稳定,阐明化疗相关的分子标志物在临床研究中依然是巨大挑战。
ERCC1最新研究 来自伦敦大学学院的李(Lee)报告了一项在晚期肺癌中依据ERCC1表达进行分层比较含铂及非铂化疗方案疗效(ET研究)的前瞻性Ⅲ期临床研究,鳞癌患者依据ERCC1表达水平高低分别接受紫杉醇+吉西他滨或顺铂+吉西他滨,非鳞癌患者根据ERCC1表达水平高低接受紫杉醇+培美曲塞或顺铂+培美曲塞化疗方案,主要终点为总生存(OS)期。研究入组648例患者,在鳞癌(177例)和非鳞癌(477例)患者中基线特征平衡。ERCC1表达采用推荐的8F1克隆号的抗体检测,在2012年补充了采用3F2克隆号的抗体同时检测ERCC1。该研究于2009年启动,2012年鳞癌患者入组停止,原因是发现不论ERCC1状态如何,非铂方案比含铂方案疗效差,两组OS分别为7.7个月对比11.2个月[风险比(HR)1.54,95%可信区间(CI)1.05~2.26,P=0.03]。
2013年终止非鳞癌患者入组,原因是发现ERCC1表达并不能作为含铂双药方案的预测因子,在ERCC1表达阳性患者中,非铂方案与含铂方案相比疗效无显著差异,OS期分别为9.7个月和10.9个月[HR1.08,95%CI0.75~1.54,P=0.68)。在ERCC1表达阴性患者中,非铂方案相比含铂方案,疗效无显著差异,OS期分别为9.5个月和8.4个月(HR0.94,95%CI0.62~1.43,P=0.79)。采用另1种ERCC1抗体(3F2)同样没能发现ERCC1与疗效相关。ERCC1对无进展生存(PFS)也无预测作用。在非鳞癌中,8F1和3F2两种抗体检出的ERCC1阳性率分别为54%和71%,存在一定的不一致性。该结果提示,依据ERCC1选择含铂或非铂化疗方案对肺癌患者OS无显著影响。
回顾相关的两项既往研究 以上研究可谓是ERCC1预测含铂化疗疗效试验再次失败,在2013年ASCO会议上,有两项化疗标志物的Ⅲ期前瞻性研究也均以失败告终。
美国韦恩州立大学卡尔马诺斯(Karmanos)癌症研究所的贝普勒(Bepler)报告的一项化疗分子标志物导向的Ⅲ期试验研究,根据RRM1和ERCC1的表达水平将患者分组,采用AQUA自动化免疫组化技术检测ERCC1和RRM1表达水平,ERCC1低/RRM1低、ERCC1高/RRM1低、ERCC低/RRM1高、ERCC1高/RRM1高4组分别给予多西他赛+卡铂、多西他赛+长春瑞滨、吉西他滨+卡铂、吉西他滨+长春瑞滨方案,各分子亚组对照组均采用吉西他滨+卡铂方案。PFS为主要观察终点。结果发现,在ERCC1和RRM1均低表达的组中,对照方案疗效优于多西他赛+卡铂方案(8.1个月对5.0个月),与预期结果相反。客观有效率(ORR)及OS在各组间无显著性差异。尽管作者认为在肿瘤化疗中的分子检测是可行的,但AQUA方法的缺陷使得结果呈假阴性。ERCC1、RRM1两个分子mRNA和蛋白表达水平无相关性。
来自西班牙的莫兰(Moran)代表西班牙肺癌协作组(SLCG)报告了另一分子标志物导向的化疗临床研究BREC,该研究根据BRCA1和RAP80的3等级分类表达水平将患者分组,BRCA1高表达者接受多西他赛治疗、RAP80低表达者接受吉西他滨+顺铂治疗、其他表达水平组合的患者采用多西他赛+顺铂治疗,未经分子标志物选择的对照组采用多西他赛+顺铂治疗。结果也是出人意料,PFS在多西他赛组为2.5个月,在吉西他滨+顺铂组为5.43个月,在多西他赛+顺铂组为5.49个月,而对照组为5.49个月。可见试验组不仅没有取得主要终点的优势,尚处于劣势(P=0.003)。作者表示,获得与预期相反的结果可能是由于对照组方案不佳以及BRCA1在鳞癌和非鳞癌中的截断(cut-off)值可能不同所致。
肺癌辅助化疗条件下的疗效预测和预后标志物
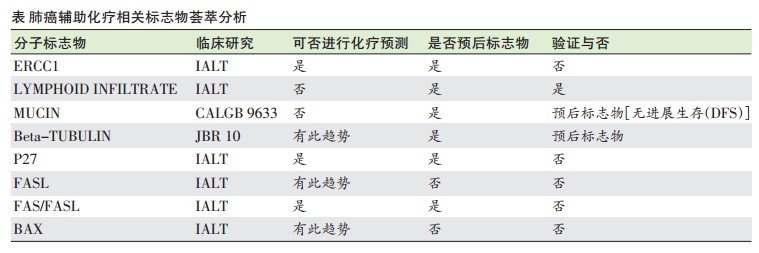
加拿大皇后大学的西摩(Seymour)报告了一项LCAEBio的荟萃分析,对肺癌辅助化疗的疗效预测和预后标志物基于4项临床研究(JBR10、ANITA、IALT、CALGB9633)的1500个样本进行了荟萃分析(下表),结果提示,尽管免疫组化法(IHC)等检测ERCC1等标志物简单、便宜,但单个临床研究的结果可能因为是错误的而将其他研究带入歧途。影响IHC检测结果分析的因素较多,包括固定方法、储存条件、应用组织芯片和单个切片的差别、长期保存还是新鲜准备切片等。他呼吁应进一步充分验证,特别是对那些正在临床研究中指导患者入组的生物标志物应更加小心关注。作者强调正开展LACEBio-2分析,将采用二代测序(NGS)技术分析辅助化疗标本,可能会更全面、可靠地分析化疗相关的预测标志物。
挑战与展望
纵观所有肺癌化疗相关标志物的转化性研究,目前尚没有一个稳定有效预测当前化疗方案疗效的分子标志物及其检测方法。这方面需要研究者重新深入思考,可能需要从药物吸收、分布、代谢及排泄(ADME)相关基因、化疗药物暴露量、DNA损伤修复通路基因、细胞骨架相关基因等角度全面分析,且可能需要整合NGS技术分析组学数据,也有可能需要建立一个由多个基因组成的有效预测标签(signature)。这些从头开始的系统性研究对于重新评价和建立化疗相关预测或预后分子标志物至关重要。
IMPRESS研究——EGFR靶向治疗耐药对策研究
研究详情: [ESMO2014]吉非替尼+化疗未改善耐药后肺癌患者PFS
来自中国香港的莫树锦(Tony Mok)教授在会议上汇报了期待已久的IM PRESS前瞻性Ⅲ期临床研究结果。表皮生长因子受体(EGFR)突变型肺癌患者接受一线靶向药物吉非替尼治疗进展后,分为两组――132例转为含铂双药化疗,133例接受吉非替尼联合含铂双药化疗。两组主要终点无进展生存(PFS)期均为5.4个月,客观有效率(ORR)分别为34.1%、31.6%。次要终点总生存(OS)尚不成熟,在靶向联合组和单纯化疗组分别为14.8个月、17.2个月。此研究结果是阴性,但有明确的临床意义,提示若患者在EGFR靶向治疗后出现耐药进展,不要盲目给予化疗联合靶向药物。吴一龙教授等专家认为该研究可能在以下设计方面存在不足,如,EGFR突变患者在耐药后的进展不同模式未区分对待以及化疗方案等;对于化疗的预测标志物分析不足也有可能是该研究未达预期结果的原因之一。
相比而言,吴一龙教授在今年美国临床肿瘤学会(ASCO)年会上报告的EGFR靶向治疗失败后的特定患者(即由MET活化所致耐药患者)采用EGFR酪氨酸激酶抑制剂(TKI)联合MET靶向抑制剂INC280的Ⅰb/Ⅱ期临床研究虽属早期试验,但明确看到了药物联合的抗肿瘤活性,ORR达17%(8/46),提示在靶点明确情况下,联用靶向药物符合药学作用机制(MOA),临床疗效可能更好。
相关解读:吴一龙教授:从ESMO研究出发谈NSCLC辅助化疗及耐药后治疗问题
会议专题》》》2014年ESMO大会专题报道
