医脉通编译整理,转载请务必注明出处。
在5月31日下午召开的ASCO全体大会上,公布了本届ASCO最重要的四项研究。其中美国纪念斯隆-凯特林癌症中心的Jedd D. Wolchok报告的一项3期研究发现,初始以Nivolumab为基础的治疗可显著提高黑色素瘤患者生存(摘要号 LBA1)。医脉通对此进行了报道。
ASCO专家Steven O’Day发表评论说:“免疫治疗药物已经为黑色素瘤治疗带来了革命性变化,现在我们看到了免疫联合治疗的威力。但是我们也应该看到,nivolumab 与ipilimumab联合也带来了更大的副作用,这可能抵消一部分患者的收益。医生和患者经需要谨慎选择,权衡利弊。”
一项III期随机试验表明单药nivolumab 或nivolumab 联合ipilimumab初始治疗的疗效显著优于单药ipilimumab。单药nivolumab治疗获得的平均疾病进展时间是ipilimumab的两倍多(6.9 个月 vs. 2.9个月),且当nivolumab与ipilimumab联合使用时患者受益更大(11.5个月)。同样nivolumab与ipilimumab联合治疗使患者获得的缓解率也得到了极大地提高,为57.6%,单药nivolumab为43.7%,而单药ipilimumab的缓解率仅为19%。
相关报道:惊奇!单剂量的免疫治疗后肿瘤消失
“在这项大型III期试验中初步观察到的联合治疗的疗效令人鼓舞,”研究的主要作者、纽约Memorial Sloan-Kettering癌症中心黑色素瘤和免疫治疗的负责人Jedd wolchok说,“另外本研究显示有特定肿瘤标记物的患者联合治疗受益最大,而其他患者联合治疗的疗效与单药nivolumab相当。这一发现将在医生为患者选择合适的治疗方案时提供重要的依据。”
Nivolumab 和 ipilimumab 均是单克隆抗体,分别阻断了不同的免疫检验点,PD-1 和 CTLA-4。这两种治疗方法,同为检验点抑制剂,从本质上提高了免疫系统抗击肿瘤的能力。
先前的研究显示免疫检验点抑制剂可以延长黑色素瘤患者和肺癌患者的生存期。ipilimumab 和 nivolumab 均是PDA 批准,可作为单药用于治疗其它药物无效的不可切除(手术不能完全切除)或转移(晚期)黑色素瘤的药物。
本研究入组了945例经治的晚期黑色素瘤患者,随机接受ipilimumab、 nivolumab 或两药联合治疗。最短随访时间9个月,中位无进展生存期ipilimumab 2.9个月,nivolumab 6.9个月,两药联合11.5个月。两药联合组与ipilimumab组、ipilimumab组与nivolumab组之间的差异具有统计学意义。
两药联合、nivolumab、ipilimumab 三组的缓解率分别为57.6%、 43.7%、 19%。联合组平均肿瘤负荷退缩率(反应程度)为52%,单药nivolumab为34%。与之相比,接受单药ipilimumab的患者肿瘤总负荷增加了5%。
与预期相同,联合组的严重药物相关副反应的发生率最高(55%),其中该组有36%的患者因副反应停药。Wolchok博士评论,先期研究已显示免疫治疗在过早停用的患者中仍有抗肿瘤效应。
这种受益延长的现象的解释是免疫治疗是通过激活免疫系统表现抗肿瘤效应,而不是直接作用于瘤体。患者需要多长时间的免疫治疗以完全激活免疫系统目前尚未明确,且各个患者需要的最短治疗时间差异较大。
本研究还收集了患者生活质量的数据,这些结果分析将在稍后报道。
PD-L1的状态可有助于确定最佳的治疗方案
免疫细胞上的PD-1蛋白可以粘附PD-L1蛋白,而PD-L1蛋白有时可见于肿瘤细胞的表面。之前有研究显示肿瘤PD-L1达到可测水平的患者,其反应率往往更佳。
本研究显示在PD-L1阳性的患者中,单药nivolumab的疗效等同于nivolumab 和 ipilimumab联合治疗。 然而,在PD-L1阴性的患者中,联合治疗的疗效显著优于单药nivolumab。
会议专题》》》2015年ASCO年会专题报道
摘要原文
LBA1: Efficacy and safety results from a phase III trial of nivolumab (NIVO) alone or combined with ipilimumab (IPI) versus IPI alone in treatment-naive patients (pts) with advanced melanoma (MEL) (CheckMate 067).
Background: The results of a phase I study in MEL suggested complementary clinical activity with NIVO (a PD-1 checkpoint inhibitor) plus IPI (a CTLA-4 checkpoint inhibitor). Here, we report the results of a randomized, double-blind, phase III trial designed to evaluate NIVO combined with IPI or NIVO alone vs IPI alone in MEL.
Methods: Treatment-naïve pts (N = 945) were randomized 1:1:1 to NIVO 1 mg/kg Q2W + IPI 3 mg/kg Q3W for 4 doses followed by NIVO 3 mg/kg Q2W, NIVO 3 mg/kg Q2W + placebo, or IPI 3 mg/kg Q3W for 4 doses + placebo, until progression or unacceptable toxicity. Pts were stratified by PD-L1 status, BRAF mutation status, and M-stage. Co-primary endpoints are progression-free survival (PFS) (reported here) and overall survival (pts continue to be followed). Secondary endpoints include objective response rate (ORR) by RECIST v1.1 and safety.
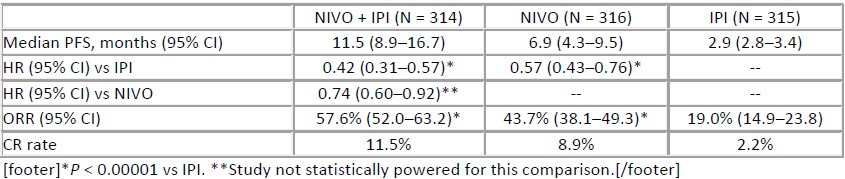
Results: At a minimum follow-up of 9 months, NIVO + IPI and NIVO alone significantly improved PFS and ORR vs IPI (Table). Grade 3-4 drug-related adverse events (AEs) occurred in 55.0%, 16.3%, and 27.3% of pts in the NIVO + IPI, NIVO, and IPI arms, respectively (most commonly diarrhea [9.3%, 2.2%, 6.1%], increased lipase [8.6%, 3.5%, 3.9%], increased alanine aminotransferase [8.3%, 1.3%, 1.6%], and colitis [7.7%, 0.6%, 8.7%]). Drug-related AEs led to discontinuation in 36.4%, 7.7%, and 14.8% of pts in the NIVO + IPI, NIVO, and IPI arms, with 0, 1, and 1 drug-related deaths, respectively. Efficacy outcomes by PD-L1 status will also be presented.
Conclusions: NIVO + IPI and NIVO alone had superior clinical activity vs IPI alone. The results with NIVO + IPI and NIVO alone further suggest complementary activity of the two agents. There were no new safety signals or drug-related deaths observed with the combination.