2014年10月11日,一场“精品”肺癌学术会议——“肺癌多学科治疗高峰论坛暨全军第六届肺癌规范化诊断治疗学习班” 在北京希尔顿逸林酒店隆重召开。
会上,广东省人民医院的吴一龙教授做了题为《回眸转化性研究,展望肺癌治疗未来》的精彩报告。现将报告的内容进行整理,以飨读者。

吴一龙教授在会议现场
精准癌医学:新方法新靶点
从分子生物学的角度看,肺鳞癌和肺腺癌是两种完全不同的癌症。肺腺癌的分子生物学的改变是以突变为主的。而鳞癌则是以基因的复制,增加为主。
C-MET的作用
我们进行的一项研究分析了在中国常见的两种非小细胞肺癌类型即EGFR突变型和EGFR野生型中,C-MET所起的作用。
研究发现,对于EGFR野生型的患者,检测到C-MET扩增或异常,意味着预后不好。但是对于EGFR突变的患者,就没有这个功能。因此二者的生物学机制是不同的。由此对于EGFR突变的患者,起主导作用的是EGFR通路,而不是C-MET通路。而对于EGFR野生型患者,C-MET通路起主导作用,扮演着重要的角色。
METLung研究是一项III期多中心随机对照试验,比较了MET受体抑制剂Onartuzumab联合厄洛替尼与厄洛替尼治疗经治性IIIb或IV期NSCLC的疗效。结果发现onartuzumab添加到厄洛替尼中并不能提高OS, PFS和总缓解率。
吴教授分析该试验失败原因,认为可能是由于在一开始就将EGFR抑制剂与C-MET抑制剂联合起来,违反了上述对C-MET作用的认识。在刚开始时,EGFR通路不扮演重要角色。
研究详情:【ASCO2014】Onartuzumab联合厄洛替尼治疗NSCLC未能获益
变换思路,C-MET抑制剂用于TKI耐药后患者
针对两个分子靶点的治疗,对第一个靶点的抑制有成瘾的作用,如果突然间断抑制,就会出现问题。因此设计试验,在检测到C-MET异常之后,可考虑继续使用EGFR-TKI并加入C-MET抑制剂。
吴教授在2014年的ASCO会议上展出的一项Ib/II期研究,就是按照这一思路设计的,结果非常令人振奋。
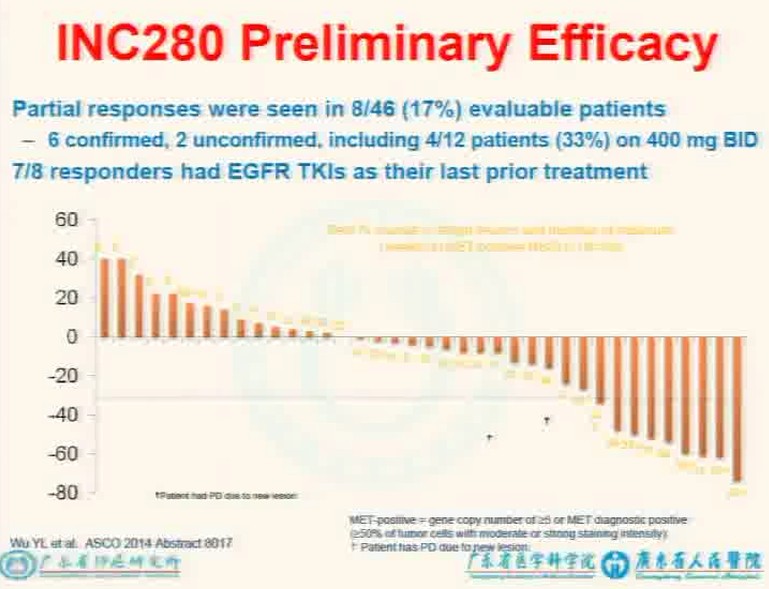
研究详情:【ASCO2014】中国研究:INC280联合吉非替尼治疗NSCLC患者的疗效
针对没有EGFR突变的患者,MET扩增分为三种,低MET水平,中度MET水平,高MET水平。对于中度及高MET水平的患者,不用EGFR-TKI,仅仅使用MET抑制剂,就可以达到很好的效果。
HER2
在过去,如果肺癌患者HER2表达阳性,则使用HER2抑制剂,但往往效果不太好。临床前的数据已经发现,当HER2发生突变之后,下面的通路PI3K-Akt同时被带动活化。
2014年ESMO大会上展出的一项研究,将Her2抑制剂Neratinib与mTOR抑制剂temsirolimus联合应用于HER2阳性的NSCLC患者,使有效率达到79%。
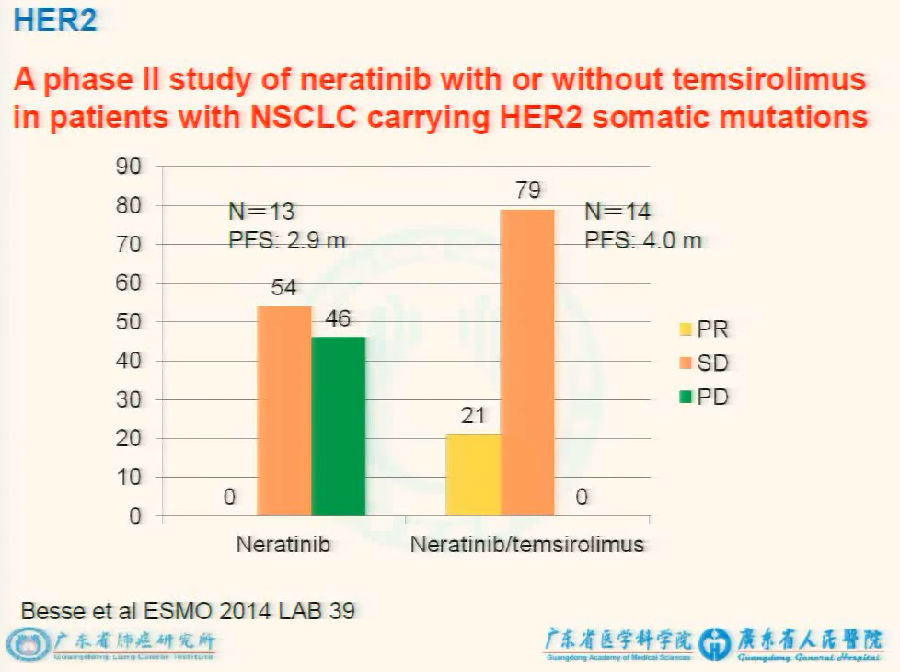
该研究突破了以往针对单个基因使用一种药物的模式,而是采用抑制旁路及下游通路的策略。
BRAF
BRAF抑制剂用于黑色素瘤效果非常好,但对于肺癌效果不佳。在2014年ESMO大会上,把BRAF进一步细分为BRAF 600E,采用dabrafenib作为其抑制剂,达到了很好的效果。
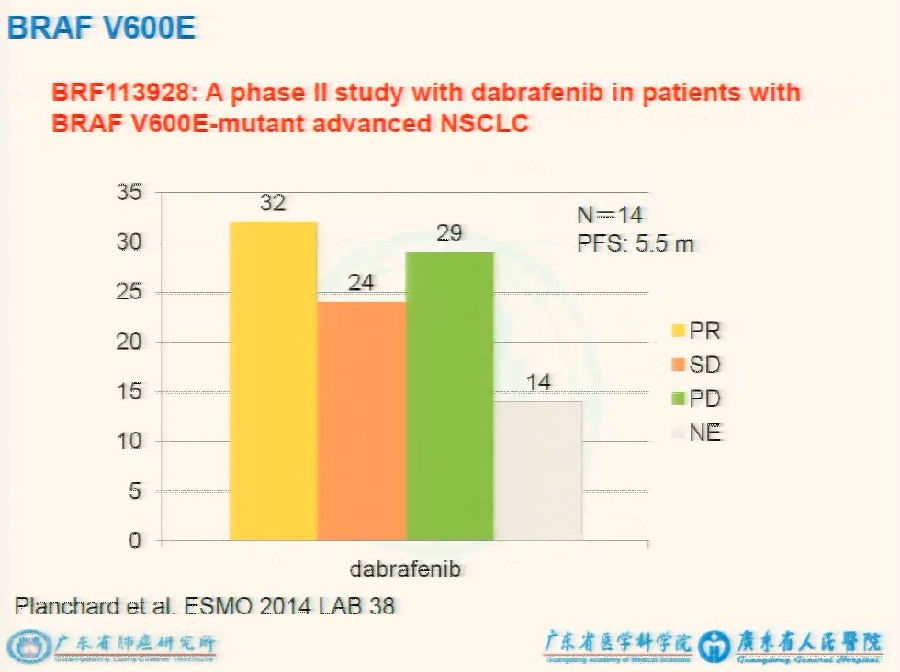
浴火重生的免疫治疗
疫苗的研究
START研究是一项国际多中心的3期研究,旨在探索在放化疗之后作为维持治疗的MUC1抗原特异性肿瘤免疫治疗tecemotide能否改善III期不可切除非小细胞肺癌患者生存。发现无法切除的III非小细胞肺癌患者在放化疗后给予tecemotide较之安慰剂,其总生存率无显著差异。
研究详情:【Lancet】肺癌免疫治疗START研究结果公布
同样,另一例免疫治疗研究MAGRIT也失败了。这一III期、安慰剂对照试验评估了MAGE-A3直接治疗后患者的无病生存。该试验在2312位IB、II期和IIIA期可以手术切除的非小细胞肺癌患者中进行。该试验中MAGE-A3阳性的患者的总生存期并未延长。
因此如果单纯的从抗炎的角度,进行免疫治疗,可能行不通。
PD-1,PDL-1靶向治疗
KEYNOTE-001研究是纳入了307例患者的Ⅰ期临床试验。研究中使用针对PD-1抑制剂的单药治疗,结果大约58%的患者可以看到肿瘤缩小,非常令人振奋。因此这条通路成为研究的新热点。
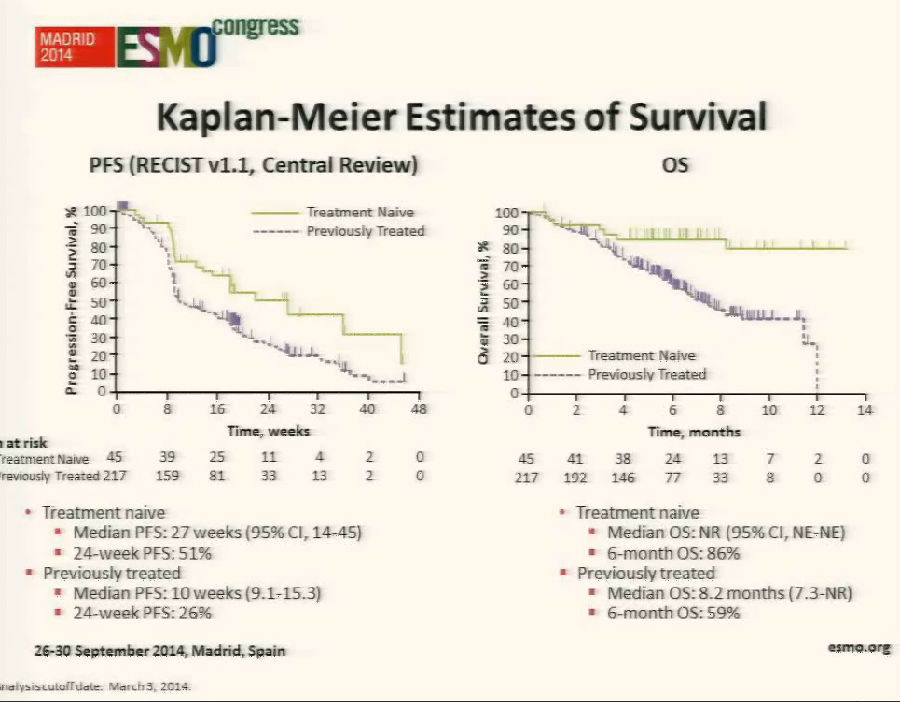
重要的临床试验汇总
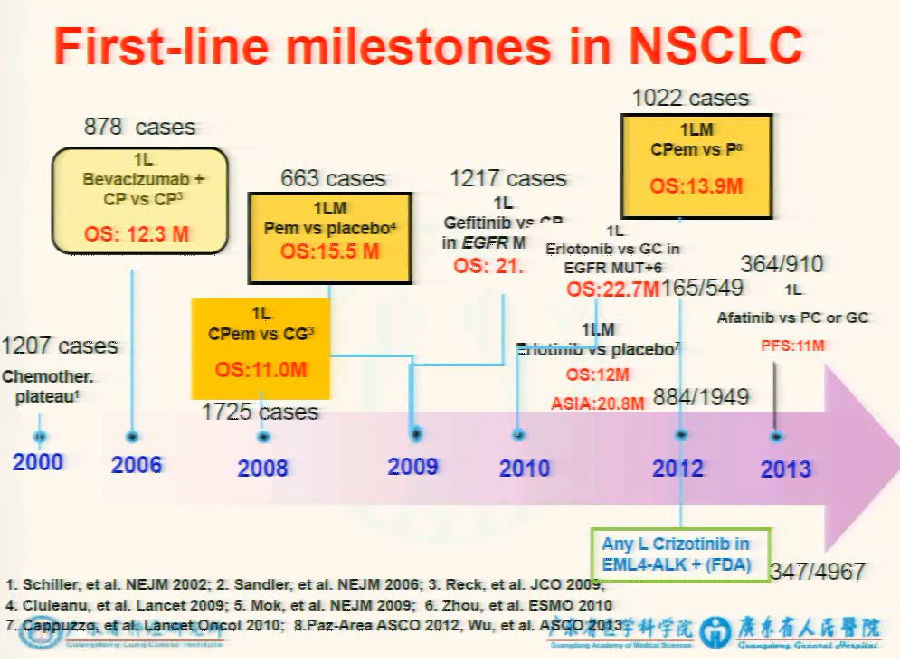
未来的治疗模式预测


更多精彩内容《《《肺癌多学科治疗高峰论坛暨全军第六届肺癌规范化诊断治疗学习班
