对于晚期非小细胞肺癌(NSCLC)的治疗,靶向联合治疗是研究的热点,但目前还没有显示出治疗结果的改善。台湾大学医学部癌症研究中心的James CH Yang教授详细分析了靶向药物联合化疗,联合血管生成抑制剂,联合新靶向药物的疗效。医脉通对此进行了报道。

James CH Yang, MD, PhD
血管生成抑制剂的联合使用
Yang博士说,目前有研究显示酪氨酸激酶抑制剂联合血管生成抑制剂具有疗效,但是需要进一步证实。
日本JO25567随机实验,将150位初次化疗的EGFR突变阳性的患者随机分配入组,进行厄洛替尼单独治疗,或厄洛替尼与贝伐单抗联用治疗。结果显示联合治疗后无进展生存时间升高了6.3个月( P = .0015;HR=0.54)[9] 。在III 期BeTa实验中,对636名经非选择性化疗的患者使用厄洛替尼或厄洛替尼联合贝伐单抗的治疗,结果发现无进展生存期没有差异,然而亚洲人群(HR=0.26)和非吸烟人群(HR=0.39)的危险率比较显著[10]。
Yang博士说:“我们应当认真研究这些实验数据,通过大型随机实验来验证结果是否正确。然而,还有一个重要的问题没有解决,即总体生存时间是否也有改善?”
与新靶向药物联合治疗
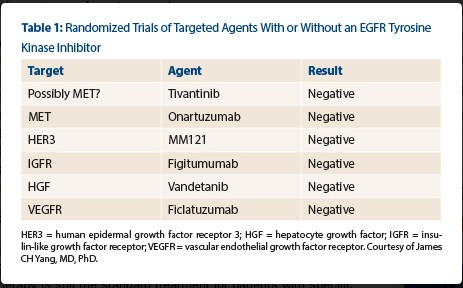
许多随机实验中,无论EGFR酪氨酸激酶抑制剂的是否联合针对另一条通路的靶向药物,结果都是阴性的(见表1)。Yang博士说:“非选择性人群可能是失败的主要原因。但是即使是在正确的人群中,不仅需要正确的突变,相关治疗靶向分子也很重要。”
举一个例子,靶向cMET治疗是很重要的。然而,对onartuzumab联合厄洛替尼治疗的全球III期MetLung实验结果不尽人意。Yang博士分析道,阴性结果可能是由于筛选病人时使用的cMET检测方法的问题。
研究详情:【ASCO2014】Onartuzumab联合厄洛替尼治疗NSCLC未能获益
他指出:“目前有许多检测cMET的方法,包括检测cMET DNA扩增的荧光原位杂交,检测mRNA含量的定量逆转录PCR,以及检测蛋白表达的免疫组化实验。我们不知道那种实验最好,也不知道驱动肿瘤细胞生长的cMET的临界值是多少。”
另外,细胞外肝细胞生长因子(cMET的配体)水平可能是干扰因素,因为这个生长因子的产生导致了EGFR突变的NSCLC的耐药。
Yang博士补充道,最近的研究结果显示,cMET的抑制剂INC280联合吉非替尼具有活性。但目前还很难下定论,因为不知道是两个药物都起作用,还是其中的一个单独起作用。要了解获得性耐药,弄清如何检测突变、选择相关的有时重叠的突变靶点,还有很多的工作要做。
举个例子,只检测EGFR突变T790M或者cMET突变,同时拥有着两种突变的患者可能就会治疗不足。有些患者,但不是全部患者,需要使用T790M突变特异性药物如AZD9291,以及cMET抑制剂如克唑替尼,或正在研发中的新cMET抑制剂。
相关报道:【ASCO2014】新药AZD9291治疗TKI耐药NSCLC显疗效
Yang博士补充道,在经EGFR酪氨酸激酶抑制剂治疗失败且T790M突变的患者中,AZD9291单独治疗显示出了疗效。今年的ASCO年会上, Jänne等人汇报了用这种方案治疗患者,发现有64%的缓解率和94%的疾病控制率。Jänne 说:“尽管我们知道会有一些cMET突变阳性的患者,我们仍然得到了很好的结果。”
Yang博士说:“对于酪氨酸抑制剂耐药的EGFR突变阳性的患者,我们需要更好方法去量化耐药生物标志物,并且克服异质性。如果想要联合靶向治疗,我们需要知道如何检测肿瘤细胞的耐药通路,从而预测哪种相关药物会起效。我们应当更巧妙的设计生物标志物驱动的试验。”
参考文献
7. Schuler MH, Yang J C-H, Park K, et al: Continuation of afatinib beyond progression: Results of a randomized, open-label, phase III trial of afatinib plus paclitaxel versus investigator’s choice chemotherapy in patients with metastatic non-small cell lung cancer progressed on erlotinib/gefitinib and afatinib—LUX-Lung 5. ASCO Annual Meeting. Abstract 8019. Presented June 3, 2014.
8. Lee CK, Brown C, Gralla RJ, et al: Impact of EGFR inhibitor in non-small cell lung cancer on progression-free and overall survival: A meta-analysis. J Natl Cancer Inst 105:585-605, 2013.
9. Kato T, Seto T, Nishio M, et al: Erlotinib plus bevacizumab versus erlotinib alone as first-line treatment for advanced EGFR mutation-positive nonsquamous non-small cell lung cancer: An open-label randomized trial. ASCO Annual Meeting. Abstract 8005. Presented June 2, 2014.
10. Herbst RS, Ansari R, Bustin F, et al: Efficacy of bevacizumab plus erlotinib versus erlotinib alone in advanced non-small-cell lung cancer after failure of standard first-line chemotherapy (BeTa): A double-blind, placebo-controlled, phase 3 trial. Lancet 377:1846-1854, 2011.
11. Spigel DR, Edelman MJ, O’Byrne K, et al: Onartuzumab plus erlotinib versus erlotinib in previously treated stage IIIb or IV NSCLC: Results from the pivotal phase III randomized, multicenter, placebo-controlled METLung (OAM4971g) global trial. ASCO Annual Meeting. Abstract 8000. Presented June 2, 2014.
12. Jänne PA, Ramalingam SS, Yang JC, et al: Clinical activity of the mutant-selective EGFR inhibitor AZD9291 in patients with EGFR inhibitor-resistant non-small cell lung cancer. ASCO Annual Meeting. Abstract 8009. Presented May 31, 2014.
医脉通编译自:Caroline Helwick,In Advanced Lung Cancer, Targeted Combinations Are Still Works in Progress,The ASCOPOST,September 15, 2014
