医脉通整理,转载请务必注明出处。
肿瘤免疫治疗是通过调动机体的免疫系统,增强抗肿瘤免疫力,从而抑制和杀伤肿瘤细胞。肿瘤免疫治疗是当前肿瘤治疗领域中最具前景的研究方向之一。这一领域的世界级专家Axel Hoos 2016年3月11日在Nature Reviews Drug Discovery杂志综述了肿瘤免疫治疗药物的发展,并对未来做出了展望。
医脉通将以系列形式为您全面详解这篇重磅综述。本文作为《三代跨越!方兴未艾的肿瘤免疫药物治疗》系列的第一部,主要包括:「肿瘤免疫治疗发展历程回顾」、「肿瘤免疫治疗研发规范」。
肿瘤免疫治疗历程回顾
通过动员机体的免疫系统抗肿瘤的概念最初可能来自19世纪中期的德国,病理学家Rudolf Virchow观察到人类肿瘤组织中出现免疫浸润。随后美国医生William Coley试图将细菌培养液(含Coley毒素)注射进无法切除的软组织肿瘤,以诱发免疫治疗反应。Coley观察到部分患者出现炎症反应而且肿瘤得以清除,而另一部分患者出现脓毒血症及并发症。由于时代的局限和对免疫机制理解的不足,肿瘤免疫治疗前进的步伐停滞了近一个世纪。
自上世纪70年代开始,包括抗体生物工程在内的科研方法和技术革新在免疫机制领域的应用,大大增加了研究者对免疫系统信号通路和靶点的认识,促进了免疫干预手段的发展。之后的30年内出现了一些免疫性的治疗方法(如细胞因子IL-2、IFN-α、刺激T细胞的疫苗等),并接受了临床试验的检验。遗憾的是这些治疗方法的效果并不理想。
免疫检查点对T细胞免疫应答的开关控制使机体免于伤害性免疫反应等基础研究的突破,为肿瘤免疫治疗带来了转折。能够动员T细胞的总开关就是CD28—细胞毒性T淋巴相关抗原4(CTLA4, 其基因于1987年被克隆)的相互作用。随后,更多的免疫检查点得到确认,如程序性细胞死亡蛋白1—程序性细胞死亡蛋白1配体1(PD1-PDL1)等。虽然CTLA4和PD1-PDL1的作用机制不同,但它们作为机体免疫应答正负驱动网络的一部分,遵循共用的基本原则。使用单克隆抗体对免疫检查点进行调控将对免疫应答产生普适作用,这一过程并不依赖于肿瘤组织学或肿瘤特异性抗原的特异性。
肿瘤免疫治疗研发规范
与传统化疗药物已建立的研发标准相区别,肿瘤免疫治疗从临床前研究向临床应用的转化需要重新构建适合其特性的药物研发样板。由知名学术研究单位、生物制药企业研发部门和多个肿瘤免疫研究协作组(CIMT、SITC、EATI、AACR)共同组成了癌症免疫治疗协会(CIC)。在基础科研和临床研发领域,CIC成员形成了一些重要的进展共识,见表1;CIC成员共同推出了针对肿瘤免疫治疗有效性、安全性临床管理的研发规范,并在Ipilimumab的研发过程得以应用,见表2。
△CIMT:the Association for Cancer Immunotherapy
△SITC:the Society for Immunotherapy of Cancer
△EATI:European Academy of Tumour Immunology
△AACR:American Association of Cancer Research
△CIC:Cancer Immunotherapy Consortium
表1. 基础科研和临床研发取得的进步
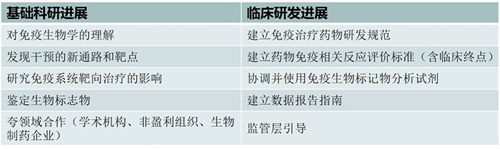
表2. CIC肿瘤免疫治疗研发规范
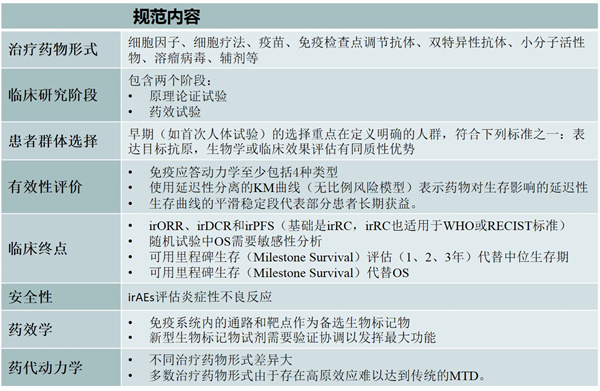
△KM:Kaplan–Meier
△irORR:免疫相关总体反应率(Immune-related Overall Response Rate)
△irDCR:免疫相关疾病控制率(Immune-related Disease Control Rate)
△irPFS:免疫相关无进展生存(Immune-related Progression-free Survival)
△irRC:免疫相关反应标准(Immune-related Response Criteria)
△RECIST:实体瘤疗效评价标准(Response Evaluation Criteria in Solid Tumours)
△WHO:世界卫生组织(World Health Organization)
△OS:总体生存(Overall Survival)
△irAEs:免疫相关不良反应(Immune-related Adverse Events)
△MTD:最大耐受量(Maximum Tolerated Dose)
图1. CIC进展共识在Ipilimumab研发项目中的应用
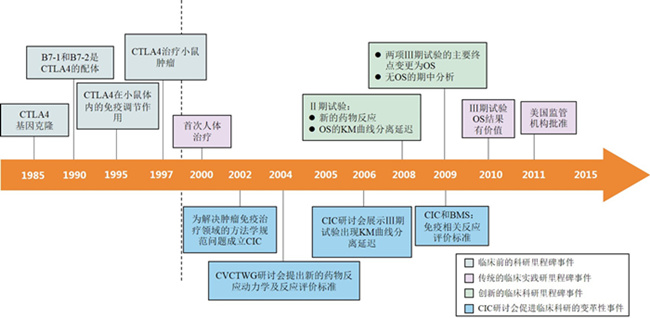
△CVCTWG:癌症疫苗临床试验工作组(Cancer Vaccine Clinical Trial Working Group)
△BMS: 百时美施贵宝(Bristol-Myers Squibb)
可用于评价临床肿瘤免疫治疗反应的标准主要有:irRC、irORR、irDCR、irPFS、Milestone Survival和irAEs。这些标准为下一代肿瘤免疫治疗方法提供了可探索的安全管理模型。CIC的成员在肿瘤免疫治疗领域发动了广泛的合作,其提供的信息作为参考被纳入美国食品和药物管理局(US Food and Drug Administration, FDA)和欧洲药品管理局(European Medicines Agency, EMA)发布的专业指南。
来源:Axel Hoos. Development of immuno-oncology drugs-from CTLA4 to PD1 to the next generations.Nat Rev Drug Discov. 2016 Mar 11. [PMID: 26965203].
图片修改自原文。
