医脉通肿瘤科用户小可真投稿
医脉通编辑一道闪电整理
众多周知,目前肿瘤基本治疗方法包括手术、放疗、化疗,以及近年来发展起来的靶向治疗和免疫治疗。而营养疗法则是贯穿肿瘤治疗始终、与基本疗法并重,改善肿瘤患者预后的重要治疗手段。本文就肿瘤营养疗法与大家共同学习。
概述
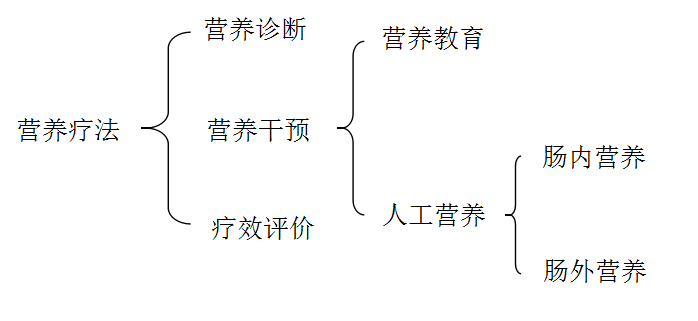
肿瘤营养疗法(cancer nutrition therapy,CNT)是计划、实施、评价营养干预,以治疗肿瘤及其并发症或身体状况,从而改善肿瘤患者预后的过程,包括营养诊断(筛查/评估)、营养干预、疗效评价(包括随访)三个阶段。其中营养干预的内容包括营养教育和人工营养(肠内营养、肠外营养)
基本概念
营养不良:一般指营养过量或营养不足,肿瘤营养不良特指营养不足。
分型:
①能量缺乏型:以能量摄入不足为主,表现为皮下脂肪、骨骼肌显著消耗和内脏器官萎缩,称为消瘦型营养不足;
②蛋白质缺乏型:蛋白质严重缺乏而能量摄入基本满足者称为水肿型营养不足;
③混合型:能量与蛋白质均缺乏者称为混合型营养不良。
常用诊断方法:(临床常以体重及BMI进行诊断诊断)
①体重诊断法:实际体重为理想体重的90%~109%适宜,80%~89%为轻度营养不良,70%~79%为中度营养不良,60%~69%为重度营养不良。
②BMI诊断法:BMI<18.5kg/m2为低体重(营养不良),18.5~23.9kg/m2为正常,24~27.9kg/m2为超重,≥28kg/m2为肥胖。
恶液质:以骨骼肌量持续下降为特征的多因素综合征。
按病因分为两类:
①原发性恶液质:直接由肿瘤本身引起;
②继发性恶液质:由营养不良或基础疾病导致。按照病程分为三期:恶液质前期、恶液质期和恶液质难治期。
诊断标准:
无节食条件下,①6个月内体重丢失>5%,或②BMI<18.5kg/m2和任何程度的体重丢失>2%,或③四肢骨骼肌指数符合肌肉减少症标准(男性<7.26,女性<5.45)和任何程度的体重丢失>2%。
肌肉减少症:进行性、广泛性的骨骼肌质量及力量下降,以及由此导致的身体残疾、生活质量下降和死亡等不良后果的综合征。
按发病原因分为原发性肌肉减少症(老化肌肉减少)及继发性肌肉减少症(活动、疾病及营养不良)。
按病程肌肉减少症分为三期,即肌肉减少症前期(骨骼肌质量减少)、肌肉减少症期(骨骼肌质量减少和力量或身体活动能力下降)和严重肌肉减少症期(骨骼肌质量减少、力量和身体活动能力下降)。
诊断标准:
骨骼肌质量减少:参照四肢骨骼肌指数符合肌肉减少症标准;(2)骨骼肌力量下降:非利手握力<40kg(男性),<30kg(女性;(3)身体活动能力下降:步速<0.8m/s。
营养评估
患者主观整体评估(PG-SGA)是目前评估肿瘤患者营养水平的首选方法。
该方法为患者自我评估+医务人员评估,内容包括体重、摄食情况、症状、活动和身体功能、疾病与营养需求的关系、代谢方面的需要、体格检查等7项,前4项由患者自己评估,后3项由医务人员评估。
评估结果分为定量评估(A营养良好、B可疑或中度营养不良、C重度营养不良)和定性评估(将7项分数相加,0~1分无营养不良、2~3分可疑营养不良、4~8分中度营养不良、≥9分重度营养不良),见图1
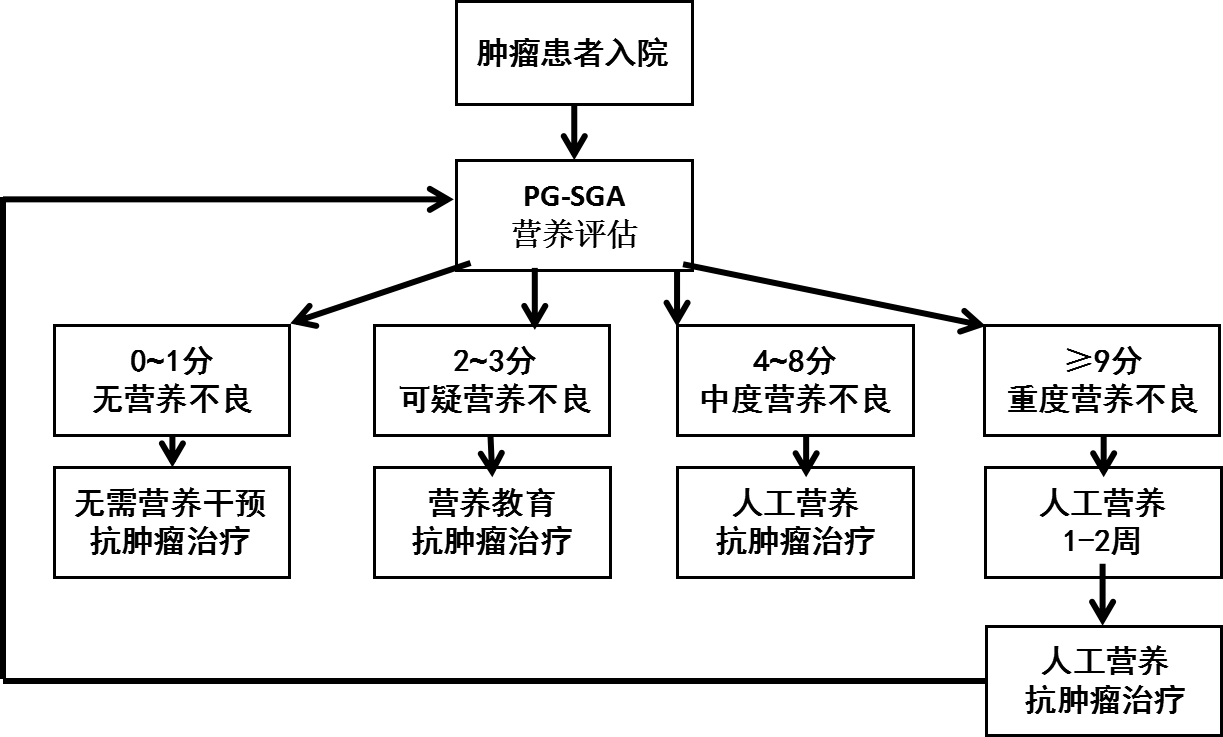
图1营养治疗临床路径
营养干预
营养干预的最高目标是代谢调节、控制肿瘤、提高生活质量、延长生存时间基本要求是满足肿瘤患者目标需要量的70%以上能量需求、100%蛋白质需求和100%矿物质及维生素需求。以下为具体标准。
能量
肿瘤患者能量如卧床需20~25kcal/(kg·d),活动需25~30kcal/(kg·d)。同时区分肠外与肠内营养,非蛋白质能量(肠外营养)按20~25kcal/(kg·d)计算,总能量(肠内营养)按25~30kcal/(kg·d)计算。
蛋白质
肿瘤患者蛋白质最少需要量为1g/(kg·d),目标需要量1.2~2g/(kg·d)。肿瘤恶液质患者总摄入量1.8~2g/(kg·d),其中支链氨基酸≥0.6 g/(kg·d),必需氨基酸≥1.2g/(kg·d)。严重营养不良肿瘤患者短期冲击营养治疗量应为2g/(kg·d);轻、中度营养不良肿瘤患者长期营养补充治疗量应为1.5g/(kg·d)。
三大营养物质比例及制剂选择
肠内营养:碳水化合物30~50%,脂肪40~25%,蛋白质30~15%;如肠外营养:碳水化合物40~60%,脂肪60~40%。
脂肪制剂:建议选择中/长链脂肪乳剂。ω-9单不饱和脂肪酸有免疫中性及低致炎症反应特点,对免疫功能及肝功能影响较小;维生素E含量丰富,克降低脂质过氧化反应。ω-3多不饱和脂肪酸有助于降低心血管疾病风险、抑制炎症反应。
蛋白质/氨基酸制剂:含有35%以上支链氨基酸的氨基酸制剂可改善肿瘤患者肌肉减少,保护肝功能,平衡芳香族氨基酸,改善厌食与早饱。整蛋白型制剂适用于绝大多数肿瘤患者。短肽制剂吸收较快,用于消化功能受损肿瘤患者。
营养不良的五阶梯治疗模式:

当下一阶梯不能满足60%目标能量需求3~5天时,应该选择上一阶梯。
营养治疗方案
针对非终末期手术患者
营养治疗并非接受外科大手术的肿瘤患者的常规措施。
中、重度营养不良患者推荐在术前接受营养治疗1~2周。预期术后7天以上仍然无法通过正常饮食满足营养需求,及经口进食不能满足60%需要量一周以上的患者,应予术后营养治疗。
开腹手术患者,无论营养状况如何,均推荐术前使用免疫营养5~7天,并持续到术后7天或经口摄食>60%需要量时为止。免疫增强型肠内营养应同时包含ω-3多不饱和脂肪酸、精氨酸和核苷酸三类底物。
需行手术治疗的患者,若合并下列情况之一:6个月内体重丢失>10%~15%,或BMI<18.5kg/m2,或PG-SGA达到C级,或无肝功能不全患者的血清白蛋白<30g/L,应在术前给予肠内营养10~14天。
任何情况下,只要肠内途径可用,应优先使用肠内营养。术后应尽早(24小时内)开始肠内营养。
针对非终末期放、化疗患者
放、化疗及联合放/化疗患者不常规推荐营养治疗。
放、化疗伴明显不良反应患者,如已有明显营养不良,则应同时进行营养治疗;放、化疗严重影响摄食并预期持续时间大于1周而不能终止,或终止后较长时间仍不能恢复足够饮食者,应予营养治疗。
头颈部肿瘤、吞咽困难、口腔黏膜炎患者管饲比口服更有效。
针对终末期患者
个体化评估及方案,当患者接近生命终点时,不需予营养治疗,仅需提供适当的水和食物以减少饥饿感。
疗效评价
营养干预的疗效评价指标
①快速变化指标:为实验室参数,血常规、电解质、肝功能、肾功能、炎症参数(IL-1、IL-6、TNF、CRP)、营养套餐(白蛋白、前白蛋白、转铁蛋白、视黄醇结合蛋白、游离脂肪酸)、血乳酸等,每周检测1~2次。
②中速变化指标:人体测量参数、人体成分分析、生活质量评估、体能评估、肿瘤病灶评估(双径法)、PET-CT代谢活性,每4~12周评估一次。
③慢速变化指标:生存时间,每年评估一次。
