医脉通编译,转载请注明出处
近期Lancet Oncology发表了LUX-Breast 1研究的结果和相关述评。该研究比较了HER2阳性乳腺癌患者一线曲妥珠单抗治疗发生进展后,二线拉帕替尼+长春瑞滨与曲妥珠单抗+长春瑞滨的效果。由于试验进行中得到的数据显示,拉帕替尼组PFS优于曲妥珠单抗组的可能性很小,且曲妥珠单抗组OS更高,数据管理委员会中止了该项研究。述评作者讨论了TKI一次次失败的可能原因以及未来在临床上可能的方向。医脉通报道。
HER2特异性单克隆抗体曲妥珠单抗在临床上的应用进展在肿瘤界是一个相当成功的故事。无论早期还是晚期HER2阳性乳腺癌患者,在化疗中加入曲妥珠单抗都能显著改善生存。尽管如此成功,曲妥珠单抗也并非对所有患者有效,在转移性乳腺癌患者中,进展是必然的。然而曲妥珠单抗甚至在进展后也存在获益。最初报道这个现象的研究1,是一项比较一线接受曲妥珠单抗为主方案并发生进展的患者,随机给予卡培他滨单药或卡培他滨+曲妥珠单抗效果的研究。与卡培他滨单药相比,继续使用曲妥珠单抗显著改善了进展时间。
HER2靶向治疗的一种替代方案是使用小分子酪氨酸激酶抑制剂(TKI),比如拉帕替尼(已获FDA批准)或尚在研究阶段的阿法替尼、来那替尼、ONT-380等。拉帕替尼获批的依据是一项研究2显示在曲妥珠单抗治疗发生进展的患者中,与卡培他滨相比,拉帕替尼+卡培他滨方案能够显著改善患者的无进展生存(PFS)。在MA.31研究中3,拉帕替尼也直接与曲妥珠单抗进行了比较。该研究比较了大部分(82%)曲妥珠单抗未经治的患者中,一线紫杉类药物+曲妥珠单抗/拉帕替尼的效果,与曲妥珠单抗组相比,拉帕替尼组PFS数据更差,同时毒性反应更多。
一个尚未解决的问题是,在曲妥珠单抗治疗发生进展的患者中,拉帕替尼或其他TKI方案与继续曲妥珠单抗方案那种疗效更好。Nadia Harbeck团队的LUX-Breast 1研究4是第一个试图解决这一问题的研究。该研究比较了一线曲妥珠治疗后发生进展的患者接受阿法替尼+长春瑞滨或曲妥珠单抗+长春瑞滨的疗效。目前,数据管理委员会中止了这项研究,因为阿法替尼能够改善PFS的可能性已经很低了,同时曲妥珠单抗组的OS显著高于阿法替尼组(风险比HR=1.48,95%CI 1.13-1.95,P=0.0048)。此外,阿法替尼方案相关毒性更大。
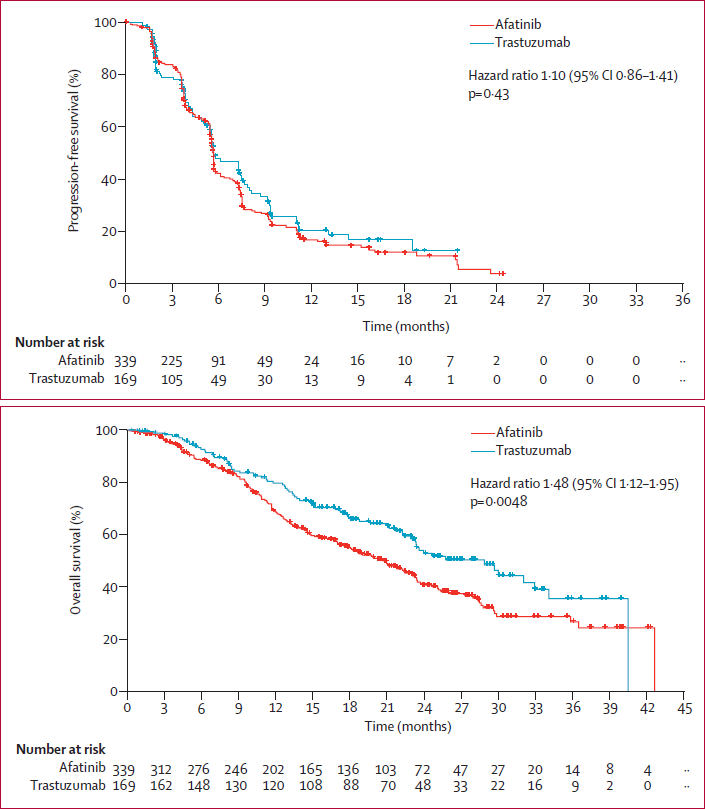
试验中止时两组PFS和OS数据(点击查看大图)
表面上看,LUX-Breast 1研究似乎只是一个显示TKI比曲妥珠单抗疗效更差,毒性更高的研究,但这个结果是很出人意料的。与拉帕替尼可逆的抑制EGFR和HER2不同,阿法替尼是一种针对全部具有激酶活性的HER蛋白(EGFR、HER2、HER4)的高度强效且不可逆的抑制剂,同时阿法替尼阻断了HER家族所有的异源二聚体和同源二聚体5。而前临床研究显示,异源二聚体,特别是HER2-HER3异源二聚体,是曲妥珠单抗耐药的重要机制之一6。因此,LUX-Breast 1的研究人员在比较阿法替尼和曲妥珠单抗时具有坚实的理论基础。人们甚至可以认为这项研究的设计是偏向阿法替尼的,因为入组的所有患者都是接受过曲妥珠单抗并发生进展的。尽管存在这些偏向,研究结果依旧是阴性的。在面对令人惊讶的数据时,回顾总结其中的经验和教训,往往更为重要。
一种可能的解释是,曲妥珠单抗除了是HER2信号通路抑制剂之外,还具有影响免疫系统的作用。这个论点的证据是,前临床研究显示曲妥珠单抗具有激活抗体依赖细胞介导的细胞毒作用的能力,这也是曲妥珠单抗在体内有效的重要机制7。一些临床研究也显示曲妥珠单抗的活性包括免疫调节活性。免疫基因标记富集的患者比没有这类标记的患者从曲妥珠单抗辅助治疗中获益更多8。尽管并非所有研究结果是都是一致的,仍有研究提示肿瘤浸润的淋巴细胞较多可以预测患者在曲妥珠单抗治疗中能够获益9。曲妥珠单抗的活性机制中,这种免疫相关的机制可能是它跨多线治疗使用仍有获益的原因。
目前的这些数据也并没有排除TKI治疗乳腺癌存在潜在作用。将TKI与曲妥珠单抗或其它靶向药物联用的方案仍在探索中。此外,一项Ⅲ期试验10显示,在曲妥珠单抗辅助治疗后,与安慰剂相比,进行1年的不可逆TKI来那替尼治疗能够改善无侵袭性疾病生存。
LUX-Breast 1研究与其它比较TKI和曲妥珠单抗疗效的研究的一致的阴性结果,明确的显示试图用TKI替代曲妥珠单抗以改善预后的方案是几乎不可能成功的。相反的,研究应当关注于改变策略,利用TKI在临床上的活性,或者与其它药物联用,或者用于特定适应症。此外,更好的理解曲妥珠单抗一次次的优于甚至最强效的TKI的原因,将会为人们带来HER2阳性乳腺癌的生物机制和耐药机制的重要信息。
参考文献:
1. von Minckwitz G, du Bois A, Schmidt M, et al. Trastuzumab beyond progression in human epidermal growth factor receptor 2-positive advanced breast cancer: a German breast group 26/breast international group 03-05 study. J Clin Oncol 2009; 27: 1999–2006.
2. Geyer CE, Forster J, Lindquist D, et al. Lapatinib plus capecitabine for HER2-positive advanced breast cancer. N Engl J Med 2006; 355: 2733–43.
3. Gelmon KA, Boyle FM, Kaufman B, et al. Lapatinib or trastuzumab plus taxane therapy for human epidermal growth factor receptor 2-positive advanced breast cancer: fi nal results of NCIC CTG MA.31. J Clin Oncol 2015; 33: 1574–83.
5. Solca F, Dahl G, Zoephel A, et al. Target binding properties and cellular activity of afatinib (BIBW 2992), an irreversible ErbB family blocker. J Pharmacol Exp Ther 2012; 343: 342–50.
6. Lee-Hoefl ich ST, Crocker L, Yao E, et al. A central role for HER3 in HER2-amplifi ed breast cancer: implications for targeted therapy. Cancer Res 2008; 68: 5878–87.
7. Clynes RA, Towers TL, Presta LG, Ravetch JV. Inhibitory Fc receptors modulate in vivo cytotoxicity against tumor targets. Nat Med 2000; 6: 443–46.
8. Perez EA, Thompson EA, Ballman KV, et al. Genomic analysis reveals that immune function genes are strongly linked to clinical outcome in the North Central Cancer Treatment Group n9831 Adjuvant Trastuzumab Trial. J Clin Oncol 2015; 33: 701–08.
9. Loi S, Michiels S, Salgado R, et al. Tumor infi ltrating lymphocytes are prognostic in triple negative breast cancer and predictive for trastuzumab benefi t in early breast cancer: results from the FinHER trial. Ann Oncol 2014; 25: 1544–50.
10. Chan A, Delaloge S, Holmes F, et al. Neratinib after trastuzumab-based adjuvant therapy in early-stage HER2+ breast cancer: 3-year analysis from a phase 3 randomized, placebo-controlled, double-blind trial(ExteNET). San Antonio Breast Cancer Symposium; Dec 8–12, 2015; San Antonio, TX, USA.
